1.目的
酢酸にイソアミルアルコール(3-メチルアルコール)を作用させて、酢酸イソアミルを合成し、これを蒸留して精製する。
2.実験器具
実験で用いた実験器具を示す。
表1 実験器具
|
品名 |
規格 |
数量 |
品名 |
規格 |
数量 |
|
三角フラスコ |
50ml |
3 |
なす型フラスコ |
100ml |
1 |
|
アリーン冷却管 |
20ml |
1 |
温度計 |
200℃ |
2 |
|
ビーカー |
200ml |
1 |
分液ロート |
100ml |
1 |
|
攪拌棒 |
|
1 |
枝付きフラスコ |
50ml |
1 |
|
ロート |
中 |
1 |
アダプター |
|
1 |
|
リービッヒ冷却管 |
20ml |
1 |
|
|
|
3.試薬・薬品
3-メチルブタノール (イソアミルアルコール) C5H12O=88.15 比重
0.8126
不快臭を有する無色の液体。
〔有害性〕 粘膜に対し刺激性、麻酔作用
酢酸 C2H4O2
=
60.05 融点
16.66 ℃ 沸点
118.1 ℃ 比重
1.0493
99 %の酢酸は低温で氷結するため氷酢酸と呼ばれる。殆どの金属類と反応して塩をつくり、アルコールと反応して酢酸エステルをつくる。
〔有害性〕 濃厚な液に触れると重い薬傷を起こす。
濃硫酸 H2SO4
=
98.09 比重
1.84
〔危険性〕爆発性,引火性いずれもないが、密閉容器内で硫酸によって鉄が侵され、
水素が発生した場合は、引火,爆発の危険性がある。また、高濃度の硫酸が有機物
と接触すると発火の恐れがある。
炭酸水素ナトリウム NaHCO3=84.01
エタノールに不溶。水溶液は加水分解して微アルカリ性を示す。
塩化カルシウム CaCl2=110.98
吸湿・潮解性がある。水に易溶。種々のアルコールやアセトンのも可溶。乾燥剤として多用されるが、アンモニア及びエタノールには適さない。
酢酸イソアミル C7H14O2=130.18 沸点
142.0 ℃ 比重
0.8719
炭化水素、エタノールなどと自由に混和するが、水に難溶。
〔危険性〕 引火性がある(引火点25℃) 冷暗所に保存
〔用途〕 塗料、印刷用インキ溶剤、各種樹脂溶剤、果実エッセンス
4.実験手順
(1)1日目
(i)100mlのなす型フラスコに3−メチルブタノール14.70gをはかりとった。
(ii)50mlの三角フラスコに酢酸12.02gをはかり、 先の3−メチルブタノールに加えた。
(iii)濃硫酸2mlをとり、器壁を伝わらせていれて、液が均一になるまで混ぜた。
(iv)実験器具を組み(図1)、沸石を入れた。
(v)油浴の温度をゆっくり125℃~130℃に上げ、おだやかに時間還流をつくった。
(vi)油を拭き、空冷してから水浴で冷却した。
(vii)別の200mlのビーカーに水18mlをいれ、それに先の反応溶液を入れた。
(viii)ロートを用いて100mlの分液ロートに入れた。そのとき沸石が分液ロートに入らないように注意した。
(ix)分液ロートを用いて、溶液のガスを抜いき、静置した。
(x)有機層と水層が分離したら、水層を取り除いた。
(xi)分液ロートに水15mlを加えた。水層と有機層を良く混ぜてガス抜きをした。この操作を2回行った。静置して、有機相と水層が分離したら、水層を取り除いた。
(xii)5%炭酸水素ナトリウム水溶液15mlを加えて、水層と有機層を良く混ぜてガス抜きをした。
(xiii)有機層を分液ロート上から乾燥した50ml三角フラスコに移し、塩化カルシウム約1gを入れて乾燥させた。
(2)2日目
(i)油浴を除いた装置(図2)を作った。
(ii)50mlの枝付きフラスコにロートを挿入して、枝の部分からの液漏れに注意しながら三角フラスコの溶液を入れた。
(iii)沸石を一粒入れた。
(iv)油浴の温度を室温からゆっくり上げた。
(v)油浴の温度を一定にした。
(vi)初めの5滴を初留としてとる。
(vii)以後を本留として重さがわかっている三角フラスコに入れた。
(viii)内部温度が下がり始めたら、加熱を止め油浴をはずした。
(ix)三角フラスコの重さをはかり、収量を求めた。
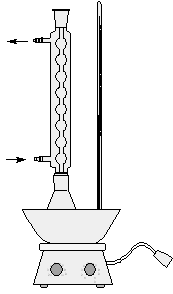
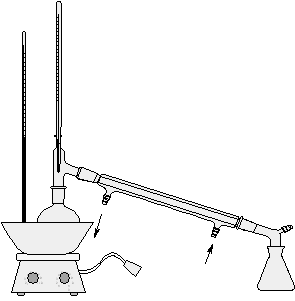
図1 反応装置 図2 蒸留装置
5.実験結果
(1)1日目(酢酸イソアミルの合成)
○イソアミルアルコールと酢酸の混合物に濃硫酸を加えた時の変化。
濃硫酸を加えたら発熱した。混合させていくと、酢酸臭が消えていき代わりにバナナのような果実臭がするようになった。
○油浴で還流中の様子
油温が100℃に達した頃から、茶色い溶液がフラスコ内の下部に溜まってきた。この時はまだ沸騰してはいなかった。この時ぐらいから、バナナのような臭いが実験台の中に充満するようになっていた(換気のスイッチは入れていた)。油温が110℃位で蒸発した気体がアリーン冷却管内に入り液化してフラスコ内に戻っていき始めた。この時は沸騰していた。
○反応物の水溶性を物質の除去
有機層は薄黄色の液体であった。水層にも若干黄色の色が付いていたようであった。この時もまた果実臭がした。
○塩化カルシウムを加えての乾燥
果実臭がして、溶液の色は薄い黄色であった。塩化カルシウムを加えると、塩化カルシウムが溶けて小さくなったように思えた。
(2)2日目(酢酸イソアミルの精製)
○初留まで
油温が134℃になったとき、フラスコの底から細かい気泡が発生してきた。フラスコ内の枝部分にある温度計は35℃であった。油温が140℃で、フラスコ内の温度37℃になったとき、沸騰が激しくなった。
油温が148℃で、フラスコ内の温度が83℃時に初留の1滴目を得た。その後、すぐに5滴採取でき、本留に入った。初留5滴目の温度は、湯浴が150℃で、フラスコ内が112℃であった。
○本留から終わりまで
初留の採取が終わるとフラスコ内の温度は少し上昇し、約130℃付近の温度を保っていた。液量が少なくなり、フラスコ内の温度が下がり始めたので蒸留を止めた。蒸留を止めた時の湯浴の温度は150℃で、フラスコ内の温度は118℃であった。
(3)収量と収率
実験に用いた各試薬の物質量を下記の表に示す。また、3-メチルブタノールと酢酸は下記の反応式のように、1対1の反応でサリチル酸を生成する。
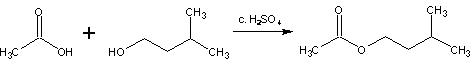
表2 試薬の物質量
|
|
3-メチルブタノール |
酢酸 |
|
採取量 |
14.70 |
12.02 |
|
分子量 |
88.15 |
60.05 |
|
物質量 |
0.1668 |
0.2002 |
上記の表より、3-メチルブタノールが限定反応物質であることがわかる。ここで硫酸を無視したのは、この反応で硫酸は触媒としてだけ関与するからである。
限定反応物質がわかったことにより、今回行った反応の収率が算出できる。酢酸イソアミルの理論収量は、限定反応物質の3-メチルブタノールの物質量に酢酸イソアミルの分子量をかけてやればいいので、
0.1688×130.19=21.710=21.71 (g)
である。よって、理論収量は21.71(g)である。
また、各操作での酢酸イソアミルの収量は下記の表のようになる。還流時の収量は、塩化カルシウムを入れて水分を除いた後の収量で、粗製物の収量に当たる。
表3 収量
|
|
三角フラスコ(g) |
全体(g) |
酢酸イソアミル(g) |
|
還流(粗製) |
― |
― |
18.24 |
|
初留 |
40.05 |
40.15 |
0.10 |
|
本留 |
33.79 |
51.12 |
17.33 |
粗製の酢酸イソアミルの収率は、
![]()
となるので、84.01%である。本留の収量を精製分と考えると、精製の収率は
![]()
となり、79.82%である。
6.考察
還流をしている際に茶色の溶液がフラスコ下部に溜まった。2日目に蒸留でも、最後まで沈殿して残っていた。今回用いた試薬の中で比重が最も重い硫酸が副反応の触媒作用をしたためであると考えあれる。副生成物は沸点が酢酸イソアミルより高く、沸点も酢酸溶液イソアミルより高い事がわかる。硫酸の脱水に伴う炭化作用では、酢酸溶液イソアミルより沸点の低いものか、ススのような比重の低いものが生成すると考えられる。よって、炭化作用以外の副反応が起きたため、茶色の比重が重い液体が生成したと考えられる。沸点の観点から見れば、3-メチルブタノールが2分子したものが考えられる。この物質の沸点は176℃である。
また、2日目の蒸留で主留沸点が130℃付近で一定に保たれていた。酢酸イソアミルの沸点は文献値では142.0℃となっている。これは、実験装置の換気設備影響などで気圧が低くなっていたために沸点が低いのだと考えられる。しかし、沸点が約10℃降下する事は考えにくい。他に考えられる原因は、フラスコ内の温度計がフラスコ内壁の近くにあったために表示温度が低くなった事である。実際に温度計がフラスコの内壁近くにあった。これはコルク栓にきちんと穴が開いていないために、温度計が傾く原因となっていた。
粗製時の溶液は薄い黄色であったが、蒸留により精製した酢酸イソアミルは無色透明の液体であった。文献には“無色透明な液体”と記述されているので、蒸留により純粋な酢酸イソアミルが得られたと考えられる。不純物が含まれていれば濁ったり、色がついたりなどするので、有意義な蒸留操作ができたと考えられる。
今実験での試薬から精製酢酸イソアミルまで合成全体の収率は約80%であった。租生成物から精製物への収率は95.0%と、蒸留で殆ど回収できた。この時の損失量は0.91gで理論収量の4.2%に過ぎない。実験全体の損失の約16%は還流時の反応時に起因すると考えられる。主な原因は、先に書いたように副生成物の生成のために、限定反応物質の3-メチルブタノールが減少した事が考えられる。
7.課題
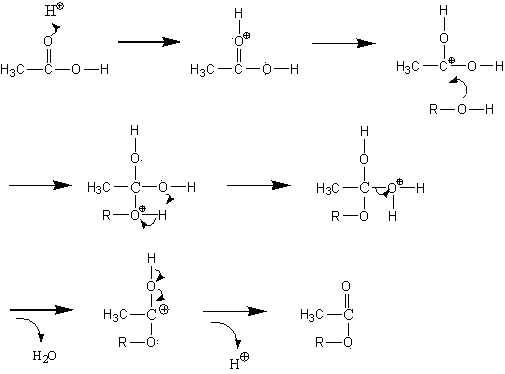
8.参考文献
フィーザー著:フィーザー 基礎有機化学,丸善,1974
フィーザー著:フィーザー 有機化学実験,丸善,1980
J.マクマリー著:マクマリー 有機化学概論,東京化学同人,2000
玉虫文一ら編集:理化学事典 第3版増補版,岩波書店,1986
http://themerckindex.cambridgesoft.com/ マルク インデックス ウェブ編