1.目的
第二級の環状アルコールであるシクロヘキサノールの脱水により、シクロヘキセンを合成し、蒸留によりシクロヘキセンの純度を上げる。そして、シクロヘキセンを用いてアルケンの反応性について学ぶ。また、n−ヘキサンの反応性と比較する。
2.実験器具と試薬
今回の実験で使用した実験器具と試薬を下記の表に示す。
表1 実験器具
|
器具名 |
規格 |
数量 |
備考 |
|
三角フラスコ |
50ml |
2 |
|
|
試験管 |
大 |
8 |
|
|
ビーカー |
100ml |
1 |
トールビーカー |
|
ロート |
|
1 |
|
|
リービッヒ冷却菅 |
|
1 |
|
|
ガラス棒 |
|
1 |
|
|
枝付きフラスコ |
|
1 |
ビグリュー菅付き |
|
温度計 |
0.1℃刻み |
2 |
100℃・200℃ |
|
分液ロート |
|
1 |
|
|
アダプター |
|
1 |
|
|
駒込ピペット |
|
1 |
|
表2 試薬
|
シクロヘキサノール |
リン酸 |
臭素水 |
|
キシレン(混合物) |
ヘキサン |
飽和食塩水 |
|
過マンガン酸カリウム水溶液 |
塩化カルシウム |
|
3.実験操作
(1)シクロへキセンの合成
(i)シクロヘキサノール20.0g,85%リン酸5ml,沸騰石を枝付きフラスコに入れ、発熱に注意しながらに二層が混ざり合うように攪拌した。
(ii)図1に示す装置を組み立て、氷浴中に三角フラスコ内にアダプターの先が入るようにした。この際、アダプターの先から蒸気が漏れないように、脱脂綿で線をした。
(iii)混合物が入った枝付きフラスコを、湯浴を用いて、150℃ぐらいまで加熱した。枝付きフラスコの残量が残り5〜10mlぐらいになったら、加熱を止め放冷を行った。
(iv)放冷し装置が触れるぐらいの温度にので、キシレン20mlと沸騰石を枝付きフラスコ内に入れた。再び加熱し、枝付きフラスコ内の残量が10〜15mlぐらいになるまで再蒸留を行った。
(v)三角フラスコ内の内容物を分液ロートに移し、三角フラスコと少量にキシレンで洗い、これも分液ロートに移した。混合物の等容積の飽和食塩水も分液ロートに入れ、油層を洗い、水層(下層)を捨てる。油層を乾燥した三角フラスコに移し、無水塩化カルシウム2gも入れ、静かな場所に静置した。(1日静置)
(vi)綿栓をしたロートで、無水塩化カリウム入れた粗留ヘキセンをろ過し、塩化カルシウムを除き、ろ液は乾燥した枝付きフラスコに入れた。粗留のヘキセンが入っていた三角フラスコを少量のキシレンで洗い、これも綿栓をしたロートを通して枝付きフラスコに入れた。
(vii)さらに沸騰石を入れ、図1の装置(三角フラスコを試験管に代えた)を組み立て分別蒸留を行った。
(viii)3本の試験管の質量を測定し、流出物を3本の試験管で採取した。温度が一定になるまでを初留分、温度一定から温度が上がり始めるまでを主留分、残りを後留分として、試験菅を分けて採取を行った
(ix)蒸留終了後、再び2本(初留と主留)の試験管の質量を量り、蒸留分の質量を算出した。
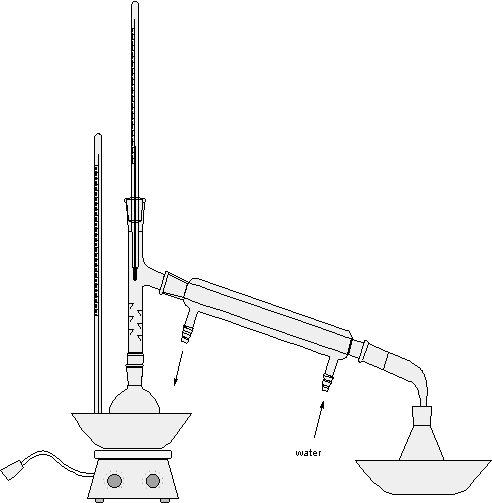
図1 反応・蒸留装置
(2)アルカンとアルケンのテスト
(i)臭素水
3本の試験菅に3%臭素水3mlずつ取り、2本にはヘキサンを1mlずつ入れ、残りの1本には精製したシクロへキセンを1ml入れ、よく振り混ぜた。次に、ヘキセンの入れた一方を光が当たらないようにドラフトの下に入れ、他方を電灯に近づけて置いた。
(ii)酸性過マンガン酸塩テスト
シクロヘキセンとヘキサンをそれぞれ試験管に1ml取り、過マンガン酸カリウム1%を加えた硫10%硫酸を一滴入れて振り混ぜた。試薬が脱色されたので、さらに試薬を加えた。最終的に5滴加えた。
4.実験結果
(1)シクロヘキセンの蒸留
(i)粗留の様子を示す
表3 粗留の様子
|
時間[min] |
蒸気温度[℃] |
油浴温度[℃] |
観察された様子 |
|
0 |
25 |
23 |
強火で加熱開始 |
|
10 |
26 |
140 |
気泡が出始めた |
|
11 |
26 |
148 |
気泡が激しく出ていた |
|
12 |
26 |
153 |
蒸気がビグリュー管内に入った |
|
13 |
30 |
156 |
蒸気がビグリュー管の上端まで昇った |
|
14 |
50 |
158 |
蒸気がリービッヒ冷却菅内に入った |
|
15 |
75 |
162 |
三角フラスコに蒸留物が入った |
|
17〜24 |
86→82 |
162 |
順調に三角フラスコ内に蒸留物が溜まっていく |
|
26 |
80 |
163 |
温度低下開始 |
|
38 |
69 |
162 |
加熱終了 |
|
40〜55 |
30℃まで |
78℃まで |
放冷 |
|
58 |
27 |
120 |
気泡が出始めた |
|
62 |
27 |
134 |
気泡が激しく出ていた |
|
64 |
40 |
143 |
蒸気がビグリュー菅の上端まで |
|
70 |
80 |
151 |
|
|
72 |
78 |
150 |
温度が一旦下がった |
|
76 |
82 |
150 |
再び温度が上昇した |
|
80 |
85 |
150 |
|
|
90 |
112 |
160 |
加熱終了 |
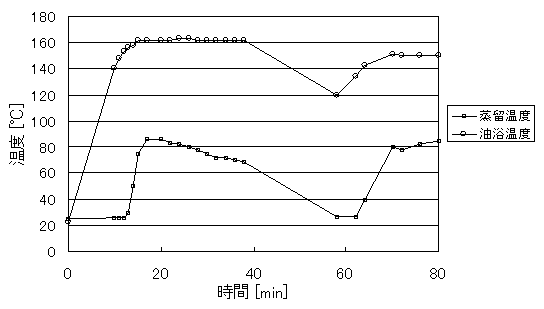
図2 粗流の時間と温度変化
注意)枝付きフラスコの径の大きさが、ビグリュー冷却菅のコルクの径より大きかった。気づいたときに、TAにこの事を伝えた。しかし、加熱してしまっていたので続けるように、と言われた。少しは止まっていたのだが、20分ごろからコルクが湿ってきて、最終的に70分ごろから枝付きフラスコとコルクの間から蒸気が漏れ白い蒸気を目で確認できるまでになった。ここでまた、TAにこの事を伝えた。加熱をしていたため、加熱を止めても蒸気が漏れているので、アルミ箔で漏れを止めてから再び加熱を始めた。
(ii)分別蒸留の様子を示す。
表4 分留の様子
|
|
時間[min] |
蒸気温度[℃] |
油浴温度[℃] |
観察された様子 |
|
初留 |
0 |
26 |
25 |
強火で加熱開始 |
|
|
5 |
26 |
98 |
気泡が出始めた |
|
|
10 |
26 |
119 |
気泡のでは激しくなった |
|
|
12 |
26 |
120 |
ビグリュー菅内に蒸気が入った |
|
|
14 |
26 |
133 |
試験管内に蒸留物が入った |
|
|
22 |
76 |
137 |
初留終了 |
|
主留 |
24 |
83 |
139 |
試験管に入る蒸留物の速度が一定に |
|
|
28 |
73 |
135 |
温度が下がり始める |
|
|
30 |
60 |
135 |
|
|
|
32 |
50 |
135 |
ビグリュー菅内に蒸気がなくなる |
|
後留 |
33 |
42 |
137 |
後留用の試験菅に 強火にした |
|
|
37 |
79 |
145 |
温度が上昇 |
|
|
46 |
90 |
153 |
温度が一定に 3mlほど溜まる |
|
|
49 |
115 |
163 |
加熱終了 |
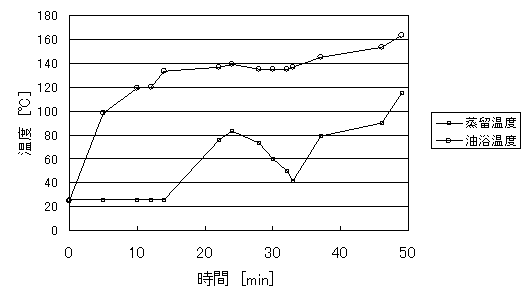
図3 分留の時間と温度
蒸気温度がシクロヘキセンの沸点に達する前から蒸留物が順調に取れ始め、80℃になる寸前で主留を始めて取り始めた。ヘキセンが前留に多く含まれていたのではないかと思う。菅内蒸気がなくなったので後留を開始した。後留はキシレン蒸気と考えたれるので、キシレンの沸点手前20℃(ヘキセンの沸点+30℃)まで加熱して終了させた。
(2)シクロヘキセンの収量と収率
(i)収量
初留と主留で回収した蒸留物の質量を示す。
表5 蒸留物の質量
|
|
試験管の質量[g] |
試験管の質量+蒸留物の質量[g] |
蒸留物の質量[g] |
|
初留 |
20.20 |
20.51 |
0.31 |
|
主留 |
20.51 |
22.65 |
2.14 |
主留で得られた物がすべてシクロヘキセンであると仮定すると、収量は2.14[g]である。
(ii)収率
上記の仮定での収量2.14[g]を用いて、収率計算をする。
シクロヘキサノールは19.98[g]であった。また、シクロヘキサノールとシクロヘキセンの分子量はそれぞれ、100.16[g/mol]と82.144[g/mol]である。ただし、分子量は理化学事典の精密な値を利用した。よって収率は、
(収率)=![]() ×100=13.
×100=13.060 =13.1 [%]
である。
(3)アルカンとアルケンの定性
変化は次のように示す。
試料を加える前 → 加えた直後 → 攪拌後
(i)臭素水テスト
○シクロヘキセン
無色透明溶液 → オレンジ色 → 上層が乳白色のにごりのある溶液で
下層が無色透明の溶液
以下のような反応式のような反応が起きたと考えられる。
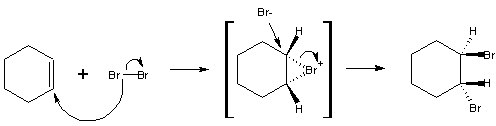
この反応は、臭素は炭素鎖の不飽和結合に付加したと考えたれる。よって、不飽和結合の検出に使うことが出来る。この実験で生成する物質は必ずトランス構造になる。
○ヘキセン
無色透明の溶液 → 上層が茶褐色の溶液で下層がオレンジの溶液
(攪拌しても変化無し)
・光を当てたもの
上層 茶褐色の溶液 → 褐色の溶液 (色が薄くなった)
下層 オレンジ色の溶液 → 黄色の溶液
色変化は、光を当てると薄くなるようであった。
・光を当てない
色の変化がない
上記の結果から、褐色の物質の臭素が光のエネルギーを得て、置換反応が起こったため臭素の濃度が減り、色が薄くなったのだと考えられる。光エネルギーを得て進むラジカル反応である。その理由は、光を当ててないものでは色の変化が見られなかったためである。
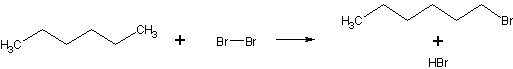
上記のような反応が進むと考えられる。しかしながら、上記の反応で示した生成物はあくまでも例の1つである。反応機構がラジカルであるため、2,3置換体などが出来き、置換する位置も不確定であるためである。
(ii)酸性過マンガン酸塩テスト
○シクロヘキセン
無色透明の溶液 → 上層が無色透明の溶液で →無色透明の溶液中に
下層は紫色の溶液 黒と茶色の中間色の沈殿
酸性の過マンガン酸塩溶液とアルケンとの反応なので、以下のような反応が起きたため、過マンガン酸イオンの紫色が消えただと思う。しかし、溶液のpHの状態が異なるとこの反応は起こりにくくなり、異なる反応が起こる。

○ヘキサン
無色透明の溶液 → 上層が無色透明の溶液で、下層が紫色の溶液
(攪拌しても変化なし)
5.考察
2日目の蒸留で生成したシクロヘキセンの純度はいいと考えられる。そう結論付けた理由は、初留を収集した際の蒸気温度が最終段階で76℃であったことが理由である。シクロヘキセンの1気圧での沸点は83℃である。この値の近い値を初留の最終段階で採取しているためである。また、反応器内の気圧は気体が発生しているので1気圧よりわずかに高いと考えられる。この事から、事実上の沸点は83℃より少し低くなると考えられる。さらに、残留している可能性がある水の沸点とキシレンの沸点より、約20℃低い蒸気温度であった。よって、初留の最終段階で採取したもの中にはシクロヘキセンが高濃度で存在していると考えたためである。
また、収率が13%と低かったのは、蒸気として反応器から逃げてしまったためだと思う。反応器から蒸気が逃げてしまった理由は、p.4に示してある。この事だけを根拠にしているわけではない。図2を見てもわかるように、蒸気温度が70〜80℃の間で緩やかな直線が長く引けているので、その間ではシクロヘキサン蒸発がビグリュー菅内にほぼ飽和していると考えられる。しかし、2日目の蒸留の温度変化を示した図3では、水平になっているどことか、70〜90℃の間で安定せず、すぐ蒸気温度が下がってしまっている。この事は、沸点が70〜90℃付近のものがなく蒸発するものがなくなり、空冷されて温度が下がっているのである。すなわち、2日目の段階ですでにシクロヘキセンが少なかったと考えたれる。これらの事をから、1日目の蒸留時に存在していたと考えられるシクロヘキセン蒸気は、冷却して凝縮する速度より、反応器外に逃げた速度が速いと考えられる。よって、シクロヘキセンは1日目の蒸留で反応器外に逃げなくなったと結論付けた。
実験書によると、最高80%の収率を得る事ができと記述されていた。今回の実験で、我々の班が13%と低かったのは蒸気の流出だけではないのかもしれない。初留を終わられた際の温度が76℃という事は、その中にシクロヘキセンがおおく含まれているという事になる。初留分すべてがシクロヘキセンと仮定しても、約15%である。よって、1日目に段階に何らかの大きな失敗をしたという事だけが明らかである。
6.課題
シクロヘキセンに冷やした過マンガン酸塩水溶液を反応させると、次の反応が起こる。
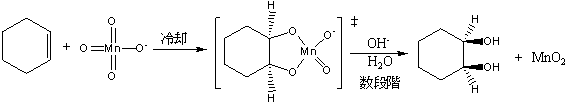 上記の反応はアルケンのシンーヒドロキシル化である。酸化される反応もあるが、その場合加熱のもしくは酸性条件下ではなくては、反応は進みにくい。上記の反応はシクロアルケンの時は、シンの付加なのでシス体ができる。
上記の反応はアルケンのシンーヒドロキシル化である。酸化される反応もあるが、その場合加熱のもしくは酸性条件下ではなくては、反応は進みにくい。上記の反応はシクロアルケンの時は、シンの付加なのでシス体ができる。
7.参考文献
フィーザー著:フィーザー 基礎有機化学,丸善,1974
フィーザー著:フィーザー 有機化学実験,丸善,1980
J.マクマリー著:マクマリー 有機化学概論,東京化学同人,2000
玉虫文一ら編集:理化学事典 第3版増補版,岩波書店,1986
http://themerckindex.cambridgesoft.com/ マルク インデックス ウェブ編