�P�D�ړI
�@�@�@�@�L�@�������w�����̏��������g�ݍ��킹�āA�A�]�F�f���������A��{������K������B�܂��A�A�]�F�f���������邽�߂ɂ̓W�A�]�J�b�v�����O�������K�v�ł���B�F�����ɂ����鋁�d�q�u�������𗘗p�����W�A�]�J�b�v�����O�����ɂ��ė�������B
�Q�D�������
����̎����ŗp���������������L�̕\�Ɏ����B
�\�P�@�������
|
�i�� |
�K�i |
���� |
�i�� |
�K�i |
���� |
|
�r�[�J�[ |
50ml |
2 |
��s�y�b�g |
2ml |
1 |
|
|
100ml |
3 |
���� |
|
1 |
|
|
300ml |
1 |
�����f�V�P�[�^ |
|
1 |
|
|
500ml |
1 |
��(�v���X�`�b�N��) |
1 |
|
|
������ |
�� |
1 |
���r�� |
|
1 |
|
|
�� |
1 |
�� |
|
1 |
|
�z���r�� |
100ml |
1 |
�~�N���X�p�[�e�� |
2 |
|
|
|
500ml |
1 |
�s���Z�b�g |
|
1 |
|
�R�� |
|
1 |
�A���~�{�[�� |
|
1 |
|
�S����� |
|
1 |
���x�v |
100�� |
1 |
|
�O�p�t���X�R |
50ml |
2 |
���X�V�����_�[ |
1 |
|
|
�u�t�i�[�R�l |
5.5cm |
1 |
�N�m�b�t�F�� |
|
1 |
|
�K���X���[�g |
70ml |
1 |
�A�[������p�� |
|
1 |
|
�K���X�_ |
�@ |
2 |
�뎆 |
�@ |
���� |
�R�D����
�@�@�@�@����̎����ŗp������������L�̕\�Ɏ����B
�\�Q�@����
|
�X���t�@�j���_ |
�@ |
�|�_ |
|
2-�i�t�g�[�� |
|
�Z���_ |
|
N,N-�W���`���A�j���� |
|
�Y�_�i�g���E���i�������j |
|
�G�^�m�[�� |
|
�����_�i�g���E�� |
|
�A�W�`�I���_�i�g���E�� |
|
���_�i�g���E�� |
|
�A�j���� |
|
���_�i�g���E���i�������j |
|
���g������ |
�@ |
�����i�g���E�� |
�S�D��������
�@(�P)�X�[�_���T�̍����Ɛ���
�@(i)���L�̂S��̗n�t�������B
�@�@ (�`)100ml�r�[�J�[�ɔZ���_�Rml���Ƃ�A�h���t�g���ŕX�₵�Ȃ���A�j����0.8ml���������������B����ɁA�X�₵10���ȉ��Ƃ����B
�@�@ (�a)100ml�r�[�J�[�Ɉ��Ɏ_�i�g���E��0.6g���Ƃ�A������15ml�������ėn�����A������X�₵��10���ȉ��Ƃ����B
�@�@ (�b)300ml�r�[�J�[�ɐ��_���i�g���E��0.5g���Ƃ�A2-�i�t�g�[��1.2g�C������35ml�������ėn�������A������X�₵��10���ȉ��Ƃ����B
�@�@ (�c)100ML�r�[�J�[�ɐ��_���i�g���E��0.5g���Ƃ�A������15ml�������ėn�������B
�@�@(ii)�t����10���ȉ��ɕۂ��āA��L�Œ��������`�n�t�����������Ȃ���A�a�t�������������Ă������B���ׂĉ����I��肵�炭���a������A���E�f�J���E���f���v�����ŃW�A�]���̏I�_���m���߂��B0.5ml���������ǂɎ��A���M���L���ƐF�̕ω��ׂ��B
�@�@�@�W�A�]�j�E�����̐����̔�����

�@�@�@���E�f�J���E���f���v�����ł̔���
�@�@�@�@�Q���h�{�Q�m���m�n�Q�{�S�g�b���@���@�h�Q�{�Q�mO�{�Q�g�Q�n�{�Q�j�b���{�Q�m��Cl
�@�@(iii) (ii)�Œ��������n�t���A10���ȉ��ɂ��Ă���b�n�t�ɓ��ꂩ���������B
�@�@(iv) (iii)�Œ��������n�t�ɁA�c�n�t�����R�O���Ԃ����������B
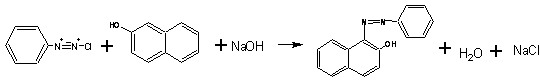
�@�@(V)�R�O�����a�����������̂��z����߂��A�ő̂𐅂Ő���B���̑�����v�R��J��Ԃ����B
(vi)���ʂ𑪒肵�������Ɍő̂��ڂ��A�����f�V�P�[�^�łP�������������B
�@�@(vii)�����������ő�(�e���X�[�_���T)�̎��ʂ𑪒肷��B
|
�}�P�@�������u |
�@�@(viii)�ő�(�e���X�[�_���T)�̂P����ʂ�A�O�p�t���X�R�ɓ���A
�@�@�@����ɃG�^�m�[��20ml���������B�O�p�t���X�R�Ɋҗ���
�@�@�@�p�Ǖt���A�E�̐}�P�̂悤�ȑ��u��g�ݗ��āA������ŗn��
��������A�n�߂͕��₵���B�n�t�������܂ʼn��������̂ŕX
�₵���B
(ix)�N�m�b�t�F����p���āA�͏o�����������z����߂����B
�@�@(x) ���ʂ𑪒肵�������Ɍő�(�����X�[�_���T)���ڂ��A�����f
�V�P�[�^�Ŋ����������B
(xi) �����X�[�_���T�̎��ʂ𑪒肷��B
�@(�Q)�I�����W�U�ƃ��`���I�����W�̍����Ɛ���
�@(�`)�X���t�@�j���_�ɃW�A�]��
�@�@(i)100ml�r�[�J�[�ɁA�X���t�@�j���_2.3g�ƒY�_�i�g���E��0.7g���Ƃ�A������25ml�ɉ��M���ėn���������B

�@�@(ii)�n�t���p���A���Ɏ_�i�g���E��1.0g�������ėn��������B���ׂėn��������A50ml�r�[�J�[�Q�ɖ�(��12.5ml)���ɕ������B�Q��100ml�r�[�J�[�ɂ��ꂼ��ɕX��6g�ƔZ���_1.5ml�����A�����50ml�r�[�J�[�̂��̂�����B�T���قǝ��a����B(�X�₵�Ȃ���A������Ƃ͍s�����B)
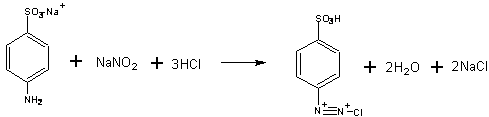
�@�@(iii)������̔������a�����������B������ώ@������A���̑���Ɉڂ����B
�@(�a)�I�����W�U�̍����Ɛ���
�@�@(i)100ml�r�[�J�[��2-�i�t�g�[��0.9g�����A10�����_���i�g���E�����n�t5ml�ŗn���������B
�@�@(ii) (�`)�Œ����������a�̂���n�t�ɁA���������Ȃ���(�a)(i)�̗n�t���������B
 �@�@(iii)���a���͏o�����̂ł��̌����D��10���ԝ��a�������A���̌㌋�����ׂĂ��n��
�@�@(iii)���a���͏o�����̂ł��̌����D��10���ԝ��a�������A���̌㌋�����ׂĂ��n��
�@�@�@����܂Œ��ʼn��M�������B
�@�@(iv)�H��2.5g�������āA����ɉ��M�����ׂĂ�n���������B�r�M���Ƃ�X�₵���B�������炢�܂ŗ₦����A���������đS�̂�����ɗ�p�����B
�@�@(v)�z����߂������B�O�a�H������100ml��p���āA�r�[�J�[���������A�u�t�i�[�R�l��Ōő̂����B
(vi)���ʂ𑪒肵�������Ɍő̂��ڂ��A�����f�V�P�[�^�łU���Ԋ����������B
�@�@(vii)�����������ő�(�e���I�����W�U)�̎��ʂ𑪒肵���B
�@�@(viii) �e���I�����W�U��100ml�r�[�J�[�Ɉڂ��A��������12.5ml�������āA���M���Čő̂��ׂĂ�n���������B
�@�@(ix)�t����80���܂ʼn����Ă���A�G�^�m�[�����25ml�������B�����āA�n�t���悭��p�����B
�@�@(x)�u�t�i�[�R�l�ŋz����߂��s�����B�r�[�J�[�͂�t�ł������A�������ׂĂ��u�t�i�[�R�l�Ɉڂ����B�Ō�ɁA���ʂ̃G�^�m�[���Ō��������B
(xi) ���ʂ𑪒肵�������Ɍő̂��ڂ��A�����f�V�P�[�^��1�������������B
�@�@(xii)�����������ő�(�����I�����W�U)�̎��ʂ𑪒肷��B
�@(�b)���`���I�����W�̍����Ɛ���
�@�@(i)�����ǂŃW���`���A�j����0.8ml�Ɛ|�_0.7ml���Ƃ�A�悭���������B

�@�@(ii) (�`)�Œ����������a�̂���n�t�ɁA���������Ȃ���(�b)(i)�̗n�t���������B10���قǝ��a�𑱂���ƒ��a���͏o���A�S���̏����Ȃ̂��ɂȂ����̂ŁA10�����_���i�g���E�����n�t9ml�������悭�����������B

�@�@(iii)���M���āA�ő̂����ׂėn���������B���₵�čr�M���������A�X�₵���B
�@�@(iv)���a���ē����܂ł悭��₵�Ă���A�z����߂������B�O�a�H������100ml��p���āA�r�[�J�[���������A�u�t�i�[�R�l��Ōő̂����B
(v)���ʂ𑪒肵�������Ɍő̂��ڂ��A�����f�V�P�[�^�łU���Ԋ����������B
�@�@(vi)�����������ő�(�e�����`���I�����W)�̎��ʂ𑪒肵���B
�@�@(vii)�e�����`���I�����W��100ml�r�[�J�[�ɓ���A������20ml���������M���Čő̂��ׂĂ�n���������B
�@�@(viii)���M���~�߁A�r�M����₵�ĒD���Ă���A���₵���B
�@�@(ix)�u�t�i�[�R�l�ŋz����߂��s�����B�r�[�J�[�͂�t�ł������A�������ׂĂ��u�t�i�[�R�l�Ɉڂ����B�Ō�ɁA���ʂ̃G�^�m�[���Ō��������B
(x) ���ʂ𑪒肵�������Ɍő̂��ڂ��A�����f�V�P�[�^��1�������������B
�@�@(xi)�����������ő�(�����I�����W�U)�̎��ʂ𑪒肷��B
�@(�R)�I�����W�U�̐��F�e�X�g
�@�@(i)���������I�����W�U0.5g�C���_�i�g���E��2g�C�Z���_�T�H����Ȃ�n�t�������B
(ii) (i)�Œ��������n�t�_�߂����M����10���قǎ����p�̕z��Z���Ă������B
�@�@(iii)�n�t������o���A���₵�A�����Ő���Ă��犣���������B
�@(�S)���`���I�����W�̎_����Y���e�X�g
�@�@(i)���`���I�����W���~�N���X�p�[�e�����ʎ����ǂɂƂ�A���ʂ̐��ɗn���������B����ɁA�_�Ɛ��_���i�g���E�������݂ɉ����ĐF�̕ω����ώ@�����B
(ii)�n�t���A���J�������āA���ʂ̈��W�`�I���_�i�g���E���������āA���M���ω����ώ@�����B
�S�D���ʂ̂܂Ƃ�
�@(�P)�X�[�_���T
�@�@(i)�����ߒ��̕ω�
�@�@�@�@�����ߒ��ł̕ω������L�̕\�Ɏ����B�܂��A�L�ڂ���Ă��Ȃ��́A���F����(���a�Ȃ�)�̗n�t�A�������͕ω����Ȃ������ꍇ�ł���B
�\�R�@�X�[�_���T�̍����ł̕ω�
|
�ߒ� |
�F |
�`�� |
���̑� |
|
|
(A) |
�@ |
���F |
������ |
�������グ�Ă��� |
|
(ii) |
�@ |
���������F |
�n�t |
���E�f�f���v�������Ŏ����������� |
|
(iii) |
�@ |
�g�F |
�Z�������t |
�E�ʏ�ɖ��̂悤�Ȃ��̖����ꕔ������ |
|
(iv) |
�@ |
�I�����W���Z�g�F |
�����S�肠�聨���炳��� |
�@ |
|
(v) |
�ő� |
�g�F�����������g�F |
���̌��� |
���O������ |
|
�@ |
��t |
�����F�����F |
�@ |
|
|
(vii) |
�@ |
��F |
���̌��� |
�@ |
|
(viii) |
�@ |
���F |
�n�t |
���S�n�������� |
|
(ix) |
�ő� |
�ΐF�ŋ������� |
�j�� |
�������Ԃ��ƍg�F(���������̐F) |
|
�@ |
��t |
�Z�������F |
�@ |
�@ |
�@�@(ii)�W�A�]�j�E�����n�t�̉��M
�@�@�@�@���������F�̉t�̂����M��i�߂�ƒ��F�ɂȂ�A����ɉ��M�����ɋ߂����F�ɂȂ����B�n�t�̔S���Ȃǂɂ͕ω����Ȃ������B�������A�t�F�����ɋ߂��Ȃ�Ə��ʼnt�L�����d���������������L���������B����͉��L�̂悤�Ȕ������i�s���A�t�F�m�[�����������ꂽ���߂ł���Ǝv���B
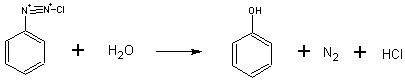
�@�@(iii)����
�@�@�@�@�X�[�_���T�̍����ł̂��ׂĂ̔������P�̉��w�������ɂ܂Ƃ߂�ƈȉ��̂悤�ɂȂ�B

�@�@�@�@����āA���̔��������牻�w�ʘ_�W�������߂���B���ۂɎ����ŗp�����ʂ��������Ă���̂ŁA���蔽�����������߂���B����玖�����L�̕\�ɂ܂Ƃ߂��B
�@�@�@���j�Z���_�Ƃ́A��ʓI�ɉ������f��39.11���ȏ�܂�ł��鐅�n�t�̂��Ƃł���B
�@�@�@�@�@�������f��39.11���܂܂�Ă��鐅�n�t�̖��x(1.200[g/ml])��Z���_�̖��x�Ƃ����B
�\�S�@�X�[�_���T�̔�������
|
�������� |
�A�j���� |
2-�i�t�g�[�� |
���Ɏ_�i�g���E�� |
���_ |
���_���i�g���E�� |
|
�̎�� |
�@0.8 [ml] |
1.26 [g] |
0.60 [g] |
3 [ml] |
0.67+0.48 [g] |
|
���x �� [g/ml] |
1.022 |
�@ |
�@ |
1.200 |
�@ |
|
���q�� [g/mol] |
93.127 |
144.17 |
68.995 |
36.461 |
39.997 |
|
������ M [mol] |
0.00878 |
0.00874 |
0.00870 |
0.0368 |
0.0288 |
|
���w�ʘ_�W�� N[-] |
1 |
1 |
1 |
2 |
1 |
|
M�^N [mol] |
�@�@�@0.00878 |
0.00874 |
�@0.00870 |
�@ 0.0193
|
0.0288 |
�@�@���j�����ł́A�L�����������Ă���B���̗��R�Ƃ��ẮA���ʂ̊e���̐��x�͂ǂ������ł���B���������Ȃ��Ƃ���ƌ����āA���萸�x�������Ȃ����߂ł���B
�@�@�@�@�\�S���A�X�[�_���T�̍����ł̌��蔽�������͈��Ɏ_�i�g���E���ł���B���Ȃ킿�A ���Ɏ_�i�g���E���P��������X�[�_���T�͂P�����ł���B
�@�@�@
�@�@�@�@�����ŁA(ii)�Ŗ�18ml�̗n�t�����珬�����ǂɖ�0.5ml����������Ƃ��l������ƁA�X�[�_���T�̗��_���ʂ͉��L�̂悤�ɂȂ�B�������A�X�[�_���T�̕��q�ʂ�248.28 [g/mol]�Ƃ���B
�@�@�@�@�@�@0.00870�~{(18-0.5)�^18}�~248.28��2.10003
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@ ��2.10 [g]
�@�@�@�@�܂��A�������ǂɖ�0.5ml��������Ƃ��������Ȃ��ꍇ�͉��L�̂悤�ɂȂ�B
0.00870�~248.28��2.16004
�@�@�@�@�@�@ �@�@�@�@�@�@ ��2.16 [g]
�@�@�X�[�_���T�͑e���E�������Ɏ����ɋl�߂Ċ����������̂ŁA���̂Ƃ��̎��ʂ����L�̕\�Ɏ����B
�\�T�@�X�[�_���T�̎���
|
�@ |
���̎��� [g] |
���{�X�[�_���T�̎��� [g] |
�X�[�_���T�̎��� [g] |
|
�e�� |
1.57 |
3.30 |
1.73 |
|
���� |
0.83 |
�@�@�@�@�@�@�@�@1.43 |
�@�@�@�@�@�@�@0.60 |
�@�@�@�@����āA�e���X�[�_���T�̎�����
�@�@�@�@�@�@�@1.73 �^ 2.16 �~ 100 �� 80.092
�� 80.1 [��]
�@�@�@�ł���B�܂��A�e���X�[�_���T���琸���X�[�_���T�ł̐������̎�����
�@�@�@�@�@�@ 0.60 �^ 1.00 �~ 100 �� 60.090
�� 60.0 [��]
�ł���B����āA�X�[�_���T�̐����܂ł̍����S�̂̎�����
�@�@�@�@�@�@�@0.801 �~ 0.600 �~ 100�@�� 48.06
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@ �� 48.1 [��]
�@�@�@�ł���B
(iv)�Z�_����
�@�@�Z�_�����(�����e���v)�őe���X�[�_���T�Ɛ����X�[�_���T�̗Z�_�𑪒肵�����ʂ����L�̕\�ɂ܂Ƃ߂��B
�\�U�@�Z�_����
|
�@ |
�P��� |
�e�� |
���� |
�Q��� |
�e�� |
���� |
|
�n���n�߂̉��x [��] |
|
110.8 |
135.8 |
�@ |
114.0 |
134.7 |
|
�n���I���̉��x [��] |
�@ |
119.7 |
139.8 |
�@ |
121.6 |
138.0 |
(�Q)�I�����W�U
�@�@(i)�����ߒ��̕ω�
�@�@�@�@�����ߒ��ł̕ω������L�̕\�Ɏ����B�܂��A�L�ڂ���Ă��Ȃ��́A���F����(���a�Ȃ�)�̗n�t�A�������͕ω����Ȃ������ꍇ�ł���B
�\�V�@�I�����W�U�̍����ł̕ω�
|
�ߒ� |
�F |
�`�� |
���̑� |
||
|
(A) |
(i) |
�@ |
���F���� |
�n�t |
�Y�_�i�g���E��������Ɣ��A |
|
�@ |
(ii) |
�@ |
�����F |
�n�t |
��p����Ɣ����V���[�x�b�g��̒��a������ |
|
(B) |
(i) |
�@ |
�W���F |
�n�t |
�E�ʏ�ɖ��̂悤�Ȃ��̖����ꕔ������ |
|
�@ |
(ii) |
�@ |
�I�����W�F |
�����S�肠�钾�a |
���a���Ɨn�t�������荇���Ă��� |
|
�@ |
(iii) |
�@ |
�����ۂ����ԐF |
�t�� |
�S���͂Ȃ��Ȃ��� |
|
�@ |
(iv) |
�@ |
�I�����W�F |
�����S�肠�钾�a |
���M����O�̏�Ԃɖ߂��� |
|
�@ |
(vi) |
�ő� |
���ꂢ�ȃI�����W�F |
���q���ׂ��� |
�S�������� |
|
�@ |
�@ |
��t |
���ԐF |
�@ |
�@ |
|
�@ |
(viii) |
�@ |
�I�����W�F |
�����n�t |
���M����Ɨn�����A���ԐF�ɂȂ��� |
|
�@ |
(x) |
�ő� |
�I�����W�F |
������ŗ��q�ׂ̍��� |
�@ |
|
�@ |
�@ |
��t |
�Ԋ��F |
�@ |
�@ |
(ii)����
�@�@�@�@�I�����W�U�̍����ł̂��ׂĂ̔������P�̉��w�������ɂ܂Ƃ߂�ƈȉ��̂悤�ɂȂ�B

�@�@�@�@����āA���̔��������牻�w�ʘ_�W�������߂���B���ۂɎ����ŗp�����ʂ��������Ă���̂ŁA���蔽�����������߂���B����玖�����L�̕\�ɂ܂Ƃ߂��B�������A(A)�ŃX���t�@�j���_�����t�����Q�ɕ�����ꂽ�Ƃ���B
�@�@�@���j�����ł��Z���_�́A�������f��39.11���܂܂�Ă��鐅�n�t�̖��x(1.200[g/ml])��Z���_�̖��x�Ƃ����B
�\�W�@�I�����W�U�̔�������
|
�������� |
�X���t�@�j���_ |
2-�i�t�g�[�� |
Na2CO3 |
NaNO2 |
���_ |
NaOH |
|
�̎�� |
2.32/2 [g] |
0.91 [g] |
0.68/2 [g] |
1.05/2 [g] |
1.5/2 [ml] |
5 [ml] |
|
���x �� [g/ml] |
�@ |
�@ |
�@ |
�@ |
1.200 |
�@ |
|
���q�� [g/mol] |
173.19 |
144.17 |
105.99 |
68.995 |
36.461 |
39.997 |
|
������ M [mol] |
0.00670 |
0.00631 |
0.00321 |
0.00671 |
0.0247 |
0.0125 |
|
���w�ʘ_�W�� N[-] |
1 |
1 |
1/2 |
1 |
3 |
1 |
|
M�^N [mol] |
0.00670
|
0.00631
|
0.0642 |
0.00671 |
0.00823
|
0.0125 |
�@�@���j�����ł́A�L�����������Ă���B���̗��R�Ƃ��ẮA���ʂ̊e���̐��x�͂ǂ������ł���B���������Ȃ��Ƃ���ƌ����āA���萸�x�������Ȃ����߂ł���B
�@�@�@�@�\�W���A�I�����W�U�̍����ł̌��蔽��������2-�i�t�g�[���ł���B���Ȃ킿�A 2-�i�t�g�[���P��������I�����W�U�͂P�����ł���B����āA�I�����W�U�̗��_���ʂ͉��L�̂悤�ɂȂ�B�������A�I�����W�U�̕��q�ʂ�350.33 [g/mol]�Ƃ���B
�@�@�@�@�@�@0.00631 �~ 350.33 �� 2.210582
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@ ��2.21 [g]
�܂��A�I�����W�U�͐��n�t���猋��������ꍇ�A�������Ƃ��ĂQ�̐����q���B���������l������ƁA�����Ƃ��ē����郁�`���I�����W�̎��ʂ�
�@�@�@�@�@�@0.00631 �~ (350.33 + 2�~18.015) �� 2.43793
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@ �@�@�@�@�@�@ ��2.44 [g]
�ł���B
�I�����W�U���e���E�������Ɏ����ɋl�߂Ċ����������̂ŁA���̂Ƃ��̎��ʂ����L�̕\�Ɏ����B
�\�X�@�I�����W�U�̎���
|
�@ |
���̎��� [g] |
���{�X�[�_���T�̎��� [g] |
�X�[�_���T�̎��� [g] |
|
�e�� |
1.62 |
4.93 |
3.31 |
|
���� |
1.59 |
�@�@�@�@�@�@�@�@3.38 |
�@�@�@�@�@�@ 1.79 |
�@�@�@����āA�e���I�����W�U�̎�����
�@�@�@�@�@�@�@3.31 �^ 2.44 �~ 100 �� 131.55
�� 132 [��]
�@�@�@�ł���B�������A�e���I�����W�U���ɂ͑�ʂ̐H�����܂܂�Ă���B�܂��A�e���I�����W�U�T���琸���I�����W�U�ł̐������̎�����
�@�@�@�@ 1.79 �^ 3.31 �~ 100 �� 54.078
�� 54.1 [��]
�ł���B����āA�I�����W�U�̐����܂ł̍����S�̂̎�����
�@�@�@�@ 1.79 �^ 2.44 �~ 100�@�� 73.360
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@ �� 73.4 [��]
�@�ł���B
(�R)���`���I�����W
�@�@(i)�����ߒ��̕ω�
�@�@�@�@�����ߒ��ł̕ω������L�̕\�Ɏ����B�܂��A�L�ڂ���Ă��Ȃ��́A���F����(���a�Ȃ�)�̗n�t�A�������͕ω����Ȃ������ꍇ�ł���B
�\�P�O�@���`���I�����W�̍����ł̕ω�
|
�ߒ� |
�F |
�`�� |
���̑� |
||
|
(B) |
(ii) |
�@ |
���I�����W�����F |
�����S���̂��钾�a�n�t |
���������Ă����ƐF���ω������B |
|
�@ |
(ii) |
�@ |
�Q�F�`�����F |
�����S���͂Ȃ��Ȃ��� |
���_���i�g���E���n�t�̓Y���� |
|
�@ |
(iii) |
�@ |
�����ۂ����F |
�n�t |
����ɔS���͂Ȃ��Ȃ��� |
|
�@ |
(vi) |
�ő� |
���F |
������� |
�ڂ��ڂ����������ł����� |
|
�@ |
�@ |
��t |
�Z�������F |
�@ |
�@ |
|
�@ |
(viii) |
�@ |
��F |
�����a���� |
���a�̓R���C�h��ɂȂ��Ă��� |
|
�@ |
(x) |
�ő� |
��������̂�����F |
�S���������Ȃ߂炩 |
�G�^�m�[�����ŋ������Ȃ��Ȃ� |
|
�@ |
�@ |
��t |
�Ԋ��F |
�����S���̂��钾�a�n�t |
�@ |
(ii)����
�@�@�@�@���`���I�����W�̍����ł̂��ׂĂ̔������P�̉��w�������ɂ܂Ƃ߂�ƈȉ��̂悤�ɂȂ�B

�@�@�@�@����āA���̔��������牻�w�ʘ_�W�������߂���B���ۂɎ����ŗp�����ʂ��������Ă���̂ŁA���蔽�����������߂���B�����̎������L�̕\�ɂ܂Ƃ߂��B�������A(A)�ŃX���t�@�j���_�����t�����Q�ɕ�����ꂽ�Ƃ���B
�@�@�@���j�����ł��Z���_�́A�������f��39.11���܂܂�Ă��鐅�n�t�̖��x(1.200[g/ml])��Z���_�̖��x�Ƃ����B
�\�P�P�@���`���I�����W�̔�������
|
�������� |
�X���t�@�j���_ |
�W���`�� �A�j���� |
Na2CO3 |
NaNO2 |
�|�_ |
���_ |
NaOH |
|
�̎�� |
2.32/2 [g] |
0.8 [����] |
0.68/2 [g] |
1.05/2 [g] |
0.7 [ml] |
1.5/2 [ml] |
9 [ml] |
|
���x �� [g/ml] |
�@ |
0.956 |
�@ |
�@ |
1.069 |
1.200 |
�@ |
|
���q�� [g/mol] |
173.19 |
121.18 |
105.99 |
68.995 |
36.461 |
36.461 |
39.997 |
|
������ M [mol] |
0.00670 |
0.00631 |
0.00321 |
0.00761 |
0.0205 |
0.0247 |
0.0225 |
|
���w�ʘ_�W�� N[-] |
1 |
1 |
1/2 |
1 |
1 |
2 |
1 |
|
M�^N [mol] |
0.00670 |
0.00631 |
0.00642 |
0.00761 |
0.02052 |
0.01234 |
0.0225 |
�@�@���j�����ł́A�L�����������Ă���B���̗��R�Ƃ��ẮA���ʂ̊e���̐��x�͂ǂ������ł���B���������Ȃ��Ƃ���ƌ����āA���萸�x�������Ȃ����߂ł���B
�@�@�@�@�\�P�P���A���`���I�����W�̍����ł̌��蔽�������̓W���`���A�j�����ł���B���Ȃ킿�A 2�W���`���A�j�����P�������烁�`���I�����W�͂P�����ł���B����āA���`���I�����W�̗��_���ʂ͉��L�̂悤�ɂȂ�B�������A���`���I�����W�̕��q�ʂ�350.33 [g/mol]�Ƃ���B
�@�@�@�@�@�@0.00631 �~ 327.34 �� 2.0659
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@ �� 2.07 [g]
�ł���B
���`���I�����W���e���E�������Ɏ����ɋl�߂Ċ����������̂ŁA���̂Ƃ��̎��ʂ����L�̕\�Ɏ����B
�\�P�Q�@���`���I�����W�̎���
|
�@ |
���̎��� [g] |
���{���`���I�����W�̎��� [g] |
���`���I�����W�̎��� [g] |
|
�e�� |
1.65 |
2.73 |
1.31 |
|
���� |
1.58 |
�@�@�@�@�@�@�@�@2.41 |
�@�@�@�@�@�@�@0.83 |
�@�@�@����āA�e�����`���I�����W�̎�����
�@�@�@�@�@�@�@1.13 �^ 2.07 �~ 100 �� 54.589
�� 54.6 [��]
�@�@�@�ł���B�܂��A�e�����`���I�����W���琸�����`���I�����W�ł̐������̎�����
�@�@�@�@�@�@�@0.83 �^ 1.13 �~ 100 �� 73.451
�� 73.5 [��]
�ł���B����āA���`���I�����W�̐����܂ł̍����S�̂̎�����
�@�@�@�@�@�@�@0.83 �^ 2.07 �~ 100�@�� 40.096
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@ ��40.1 [��]
�@�ł���B
�@(�S)�I�����W�U�ł̐��F
�@�@�@�@�I�����W�U�𐅂ɗn�����ƁA�n�t�̐F�͐Ԃ��Ȃ����B���M�����āA�n�t���琅���C�������オ��n�߂��̂ŁA�����p�̕z(�K�[�[)����ꂽ�B����������A�K�[�[��n�t��������o���ƃI�����W�F�ɐ��F���ꂽ�B���~�߃K�[�[�𗬐��ł������ł����ƁA�K�[�[�̐F�����������ĉ��F�݂��������I�����W�F�ɂȂ����B
�@(�T)���`���I�����W�̎_����e�X�g
�@�@�@�@�������������`���I�����W�́A���F�ɃI�����W�������������悤�ȐF�ł������B������X�p�`�����ŋɏ��ʂ��̎悵��Rml�̐��ŗn��������ƁA�n�t�̐F�̓I�����W�F�ƂȂ����B�����ɁA�_���P�H������Ɛԓ��F�`�������Ԏ��F�ɂȂ����B�����ɁA���_���i�g���E�����n�t���P�H������ƁA�n�t�̐F�͂قڌ��̃I�����W�F�ɂ��ǂ����B����ɁA���_���i�g���E�����n�t���P�H������ƁA�n�t�̐F�͐�قǂ̃I�����W�F��菭�����F���ۂ��Ȃ����B
�@�@�@�@�_���n�t���ŁA���`���I�����W�n�t���Ԃ��Ȃ����͈̂ȉ��̔����ŋ����N�����Ă��邽�߂ł���B���̋������F�̌����ł���B

�@�@�@�@����ɂ����n�t�Ɉ��W�`�I���_�i�g���E���������ĉ��M���Ă����ƁA�n�t�̐F�͂ǂ�ǂ��Ȃ��Ă����A�Ō�͊��S�ɖ��F�����Œ��a�̂Ȃ��n�t�ɂȂ����B���̔����́A���̃y�[�W�ɂ��锽�����i���߂ł͂Ȃ����Ǝv���B
�@�@�@�@���̍����̓W�A�]�j�E�������L�̐Ԍn�̐F�����������߁AN-N�̓�d�������Ȃ������ƍl�������߂ł���B����ɁA���W�`�I���_�C�I���͊Ҍ��܂ł��邩��ł���B
�@�@�@
�@�@�@�@�@�܂��A���F�ɂȂ����n�t�����w�Ɛ��w�œ�w�ɂȂ�Ȃ������̂́A�����������ƍl�����鉻�����A�X���t�@�j���_�i�g���E���Ƃ��|�A�~�mN,N�[�W���`���A�j����(N,N-dimethylbenzene-1,4-diamine)���C�I�����̊��\��������Ă���ƍl�����B������������n�t�ł̓A�~���n�����͗V������Ă��܂��̂ŁA������������\�������邪�A�n�t�̔Z�x���������ߐ��n�t���ɗn���Ă��܂����ƍl������B
�T�D�l�@
�@�@�@�X�[�_���T�̈�A�̍����ߒ��ŁA�e���̎�������80���ƍ��������̂́A�����̗��q���ׂ����A���������S�ɏ����������������S�Ɋ������Ă��Ȃ��������߂ł͂Ȃ����Ǝv���B�����f�V�P�[�^�ɔ����������ꂨ�炸�A���ڂɂ��������܂�ł���悤�Ȋ���������ꂽ�B���ۂɑe�����̑傫�ȉ���ӂ����Ƃ��̊�������A�����𑽏��܂�ł���悤�Ȋ����ł������B����͑e�������琸�����ւ̎�������60���ł��������Ƃł�������B���̂Ƃ��͖�P�T�Ԍ����f�V�P�[�^���Ŋ����������߁A������Ɛ�������ꂽ�߁A�������Ⴍ�Ȃ����̂ł͂Ȃ����Ǝv���B�����܂ł̍����ߒ��S�̂̎�������50���ƒႩ�����̂́A�W�A�]�j�j�E�����������������߂ł͂Ȃ����Ǝv���B���̂��߁A�W�A�]���ȍ~�̔������N���邱�Ƃ��o���Ȃ��������ߎ��������������B�Z�_����ł́A�e�����E���������Ɍ������n���n�߂̉��x�Ɨn���I���̉��x�����傫�������B����͌������Z�����n�߂����ɁA���x�㏸�𐧌䂷�郌���W��ς����ɉ��M�������Ă��܂������߂ł���B���S�ɗZ�����m�F���Ă���Ԃɂ����x���㏸���Ă��܂����B�������A�e�����̗Z�_�����������̗Z�_���̂Q�{�ł���A�e�����̗Z�_�͐������̗Z�_����Q�O���Ⴉ�����B���̂��Ƃ���A�e�������̐������̕����X�[�_���T�̏��x�͍����Ƃ�����B
�@�@�@�I�����W�U�̑e�����̎�����100�����Ă���̂��A�X�[�_���T�Ɠ��l�Ɋ����������e���̌����ɑ����̐������܂�ł��邽�߂��Ǝv���B����͌����̗��q���ׂ�����������ɂȂ��Ă����̂��v���̂ЂƂł��낤�B�������Ȃ���A�U���Ԍ����f�V�P�[�^�Ŋ����������̂Ő����𑽂��܂�ł���Ƃ͍l���ɂ����B�������Ƃ��ăI�����W�U�ɕt���ĉ\�͍l������̂ŁA���������Q���q�ȏ�t���Ă���̂ł͂Ȃ����낤���B����ɖO�a�H���������ăI�����W�U�����͂����ۂɁA�I�����W�U�����ł͂Ȃ����n���̕��������܂ł����͂��ꂽ�̂��낤�B�܂��H���̓i�g���E���C�I���̋��ʃC�I�����ʂŐ͏o���A������e�����Ɋ܂܂�Ă����̂��낤�B�����ōČ����������Ƃ��ɁA�e�����Ŋ܂܂�Ă����H���ȂǂƐ��n���̕��������͂Ȃ��Ȃ�A�G�^�m�[�����ł͌������Ƃ��ăI�����W�U�Ƌ����������Ă��鐅�ȊO���������B����āA�e�������琸�����܂ł̎�������T���Ȃ̂ŁA�����s�����������ƍl������B�������A�����܂ł̍����ߒ��S�̂̎�������V���ƍ������ɂȂ����B����͐������������f�V�P�[�^�ɔ�����������Ă��炸�A���S�ɐ�����G�^�m�[�������������Ɋ������\���ɍs���Ă��Ȃ��������߂ł͂Ȃ����낤���B
�@�@�@���`���I�����W�̑e�����̎�������55����Ⴉ�����B����͓������ɍ������s�����I�����W�U�Ƃ͋t�̌��ʂł���B���`���I�����W���I�����W�U�Ɠ��������Ő������܂�ł���ƍl����ƁA�e�����琸���܂ł̎����̓I�����W�U�Ƃقړ������Ȃ�͂��ł���B���������ۂ͈قȂ�A��V���Ƃ����������ł������B�����̎�����A����������������I�����W�U�ƈꏏ�Ȃ̂ŁA�I�����W�U�̊����������e���ɂ͐����͂��܂�܂܂�Ă��Ȃ��������ɂȂ�B�܂��A�����܂ł̍����ߒ��S�̂̎�������S���Ƃ��������ɂȂ����B�������������f�V�P�[�^�ɔ�����������Ă��Ȃ��̂ŁA���ۂɂ͊��S�ɐ������������Ɋ��S�Ɋ������s���Ă��ƍl����ƁA���Ȃ�Ⴂ�����ɂȂ�B�����Ȃ��Ă��܂��������̓X�[�_���T�̂Ƃ����l�ɁA�W�A�]�j�j�E�����������������߂ł͂Ȃ����Ǝv���B
�@�@�@
�U�D�ۑ�
�@�@(�P)�X�[�_���T�����F�Ɍ����Ȃ����R
�@�@�@�@�@���F�͊�{�I�ɁA�������q�̃C�I�����������@�ە��q�̃C�I�����ƌ������邽�߁A�@�ۂɐ������蒅����B�������@�ۂ��C�I�������������Ă��A�Z�����[�X�@�ۂ���F�ł��Ȃ����̂�����B
�@�@�@�@�@�ǂ���ɂ��Ă��A�X�[�_���T�ɂ̓C�I�����̊��\��Ȃ��B����āA���̂��ߐ��F�܂Ƃ��Ă͌����Ȃ��B�������A���U�����Ƃ��Ă͗p���邱�Ƃ��ł���B
�@�@
(�Q)���`���I�����W�ƃI�����W�U����������ۂɁA�A�]�J�b�v�����O���s�킹������(���g)���قȂ����B���̎��ɂ��āA�t�F�m�[���C�A�~���C�W�A�]�j�E�����̊e�����ł̍\���Ɋ�Â��A������ω������čs�������R���������B
�@�@�@�@�܂��A�t�F�m�[���C�A�~���C�W�A�]�j�E�����̎_���Ɖ���ł̍\���������B�������A����̃A�]�J�b�v�����O�����͖F�����̋��d�q�u�������̂P�ł���̂ŁA�A�~���̓A�j�������A�W�A�]�j�E�������n���Q�����x���[���W�A�]�j�E�����������B�����ł́A�w�̓n���Q�����f�ł���B
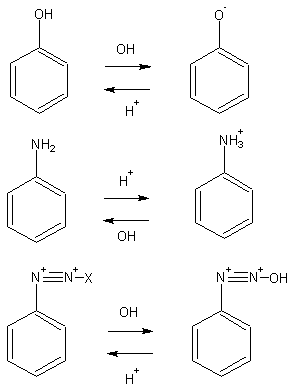
������n�t���ł̃t�F�m�[���́A���f����o���t�F�m�L�V�h�C�I���ɂȂ�B�t�F�m�L�V�h�C�I���͎_�f���}�C�i�X�̓d�ׂ�ттĂ���̂Ńx���[���ɓd�q�����^���āA�J���{�J�`�I�����ԑ̂���r�I���艻�����B�������A���j����̍U�����I���g�ʂƃp���ʂɋN����Ɣ�r�I�Ȉ���ȃJ���{�J�`�I�����ԑ̂���퐶�������B������ǂ��A�Q�|�i�t�g�[���ł̓L�h���L�V����̃p���ʂɂ͒u�����N���������o���Ȃ��̂ŁA�I���g�ʂɒu�����N�����B�u�������ʂɕt�����������ʂɕt��������葽���̋��\������������B���Ȃ킿�A����ȉ������Ȃ̂ŁA���ʂɒu�����N����B
�܂��A�_�����n�t���ł̃A�j�����́A���f�����f�C�I���ăA�j�����C�I���ɂȂ�B�@���̃C�I���͐��d�ׂ������Ă��邽�߁A�x���[������d�q���z�����邽�߃J���{�J�`�I�����ԑ̂��s���艻�����B���̂��ߖF�����̋��d�q�u�������͕s�����������B�������A���j����̃��^�ʂւ̍U���Ő�����J���{�J�`�I�����ԑ̂��ł�����ƂȂ�B����āA���`���I�����W����������Ƃ��́A�_�����ɏ������ɂ���N, N-�W���`���A�~����i(H3C)2N�[�j�̃��^�ʂŃA�]�J�b�v�����O�������鎖�ɂ��A�ړI�̃��`���I�����W�������ł���B
�����A����͒u�����N����ʒu�̋c�_�ɂ��������Ȃ��B�{���I�ȃW�A�]�j�E�����̔������́A����������_�������̕����悢�B�����A����������Ŕ������������̂ł���A�o���邾���㉖��̏������Ŕ���������̂��D�܂������ɂȂ�B��ɏq�ׂ��悤�ɁA�t�F�m�[��������ŏ���������ƁA�}�C�i�X�̓d�ׂ����t�F�m�L�V�h�C�I���ɂȂ�B�t�F�m�L�V�h�C�I���̓t�F�m�[�����x���[���ɓd�q�����^���₷���B���Ȃ킿�A�t�F�m�L�V�h�C�I���̕����������͍����B�������A�^���������]�܂�������Ƃ����āA�_�𑽂�����Ǝ�_�ł���t�F�m�[�����V������ăt�F�m�L�V�h�C�I�������Ȃ��Ȃ��Ă��܂��B���Ȃ킿�A�_���x���ア�������悢�B�����Ƃ����āA����ɂ���ƃJ�b�v�����O�������N���Ȃ��Ȃ��Ă��܂��̂ŁA�o���邾���ア����̏������Ŕ���������̂��œK�ł���B
�A�~���ł���A�j�����̏ꍇ�����l�ŁA�_�ŏ�������ƁA���d�ׂ��v���X�̓d�ׂ�ттĖF�����̋��d�q�u�������̔�������ቺ�����Ă��܂��B����āA���_���������ł͂�葽���̃A�~�����v���X�̓d�ׂ�ттĂ��܂��̂ŁA�x���[������d�q���z������ĕs�����ɂȂ�A�J�b�v�����O�����̑��x�������Ă��܂��B����āA���̏ꍇ�͎�_���������Ŕ�����i�߂邪�]�܂����B
�V�D�Q�l����
�@�@�����\���C�{�C�h�����F���f�\���{�C�h�@�L�@���w(��)�C�������w���l�C1989
�@�@�@�@�t�B�[�U�[���F�t�B�[�U�[�@��b�L�@���w�C�ۑP�C1974
�@�@�@�@�i�D�}�N�}���[���F�}�N�}���[�@�L�@���w�T���C�������w���l�C2000
�@�@�@�@�ʒ������ҏW�F�����w���T�@��R�ő���ŁC��g���X�C1986
�@�@�@�@http://themerckindex.cambridgesoft.com/�@�}���N�@�C���f�b�N�X�@�E�F�u��
��c����璘�F�}���ƃt���[�`���[�g�ɂ��V�L�@���w�����C�Z�o�ŁC2001
